慢性肾病(CKD)是一种日益严峻的全球健康问题,其患病率呈逐年上升趋势。随着疾病进展,肾脏与肠道之间的相互作用引起了越来越多研究者的关注。肾-肠轴这一概念的提出,为我们提供了一种全新的视角,揭示了肠道微生物群失调与慢性肾病之间的深刻联系。慢性肾病的治疗不仅仅局限于肾脏本身的病理改变,肠道健康与微生物群的平衡同样在疾病的发生与进展中起着重要作用。如何通过调节肠道微生物群来减缓肾脏损伤,成为当前研究的热点。
肾-肠轴:肾脏与肠道的紧密联系

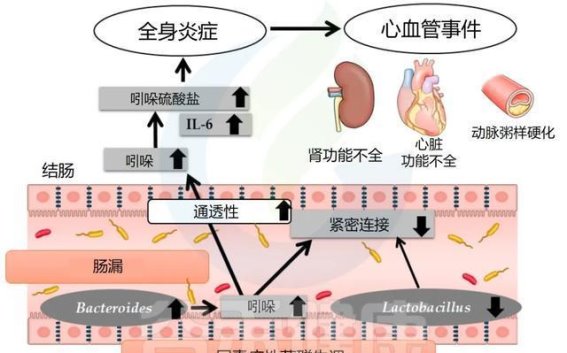
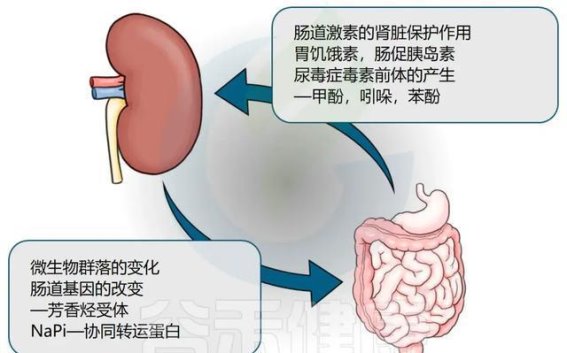
近年来的研究揭示了肾脏与肠道之间的复杂相互作用,肾-肠轴不仅仅是两者之间的物理联系,更是通过生理机制相互调节的系统。肠道不仅仅是食物消化的场所,它还通过细菌代谢产物影响肾脏功能。研究发现,慢性肾病患者的肠道菌群通常表现为失调,肠道通透性增加,肠道细菌及其代谢产物进入血液后,对肾脏产生负面影响。这一过程不仅加剧了尿毒症毒素的积累,还引发了肾脏的慢性炎症反应,从而加速了疾病的进展。
肠道内的菌群失衡与尿毒症毒素的过度生成密切相关。像吲哚硫酸盐(IS)和对甲酚硫酸酯(pCS)这样的毒素,是由肠道细菌代谢产生的,它们会通过血液进入肾脏,导致氧化应激和炎症反应的加剧。这些毒素的增加,尤其是在肾脏功能下降时,往往会引起心血管并发症的发生。肠道菌群的改变与肾脏损伤之间存在恶性循环,这一循环的存在,进一步加剧了慢性肾病的病理发展。
微生物群调节:治疗的新兴方向

微生物群调节,特别是益生菌、益生元以及后生元的应用,已经成为慢性肾病治疗中的一项新兴领域。通过调节肠道内的微生物群,尤其是增强有益菌的数量,我们可以改善肠道的功能,降低尿毒症毒素的生成,从而减轻肾脏负担。尽管现有的临床研究显示益生菌在改善肠道菌群平衡方面有所成效,但其对肾功能和生存率的改善效果仍然缺乏足够的证据。
益生菌通过促进肠道内有益菌的生长,有助于维持肠道的健康。临床研究结果并不一致,部分研究显示,益生菌能降低尿毒症毒素水平,但对肾功能的改善并不显著。以乳酸杆菌和双歧杆菌为代表的益生菌,在一些慢性肾病患者中表现出了改善铁代谢、减轻炎症的作用,但这些作用对于肾小球滤过率(eGFR)的改善并不明显。益生菌的疗效仍然需要更多的临床试验来验证。
后生元作为益生菌代谢的产物,近年来也逐渐被提到治疗慢性肾病的新策略中。短链脂肪酸(SCFAs)是后生元中的重要成分,已被证明具有抗炎作用,并能通过调节肠道免疫系统来减轻慢性肾病的症状。研究显示,SCFAs有助于维持肠道屏障功能,抑制肠道炎症,进而减轻肾脏的损伤。后生元作为一种新的干预手段,或将成为治疗慢性肾病的潜力方案。
饮食干预:低蛋白和高纤维的双重作用
饮食干预在慢性肾病治疗中的作用不可忽视。低蛋白饮食是慢性肾病治疗中的一种传统方法,近年来,研究证明,低蛋白饮食能够有效减缓肾脏功能的下降。蛋白质的限制可以降低肾脏的代谢负担,减少尿毒症毒素的积累,从而减轻肾脏损伤。与益生元联合应用,低蛋白饮食还能进一步改善肠道菌群,增加有益菌的数量,降低尿毒症毒素水平。

低蛋白饮食的实施并非没有争议,部分研究提出,低蛋白饮食可能导致慢性肾病患者的营养不良或肌肉消耗。幸运的是,最新的研究表明,在摄入足够能量的情况下,低蛋白饮食并不会导致这些负面影响。相反,它能够有效改善代谢性酸中毒,并减缓肌肉退化。在保证能量摄入充足的前提下,低蛋白饮食是慢性肾病患者的一个有效治疗选项。
高纤维饮食也显示出对慢性肾病患者的益处。膳食纤维通过促进肠道有益菌的生长,增加短链脂肪酸的产生,从而改善肠道屏障功能,降低肠道通透性。这一过程有助于减轻肾脏的炎症反应,降低心血管事件的发生风险。高纤维饮食应当成为慢性肾病患者的常规饮食组成部分,帮助其维持肠道健康。
非抗生素药物的影响:药物与肠道菌群的互动
除了传统的益生菌和饮食干预,非抗生素药物对肠道微生物群的影响也受到越来越多的关注。例如,SGLT-2抑制剂是一类降糖药物,它通过抑制肾脏对葡萄糖的重吸收,帮助降低血糖。研究表明,SGLT-2抑制剂不仅能够改善糖尿病患者的血糖控制,还能通过调节肠道微生物群的结构,改善肠道功能。卡格列净作为SGLT-2抑制剂的一种,已被发现能够提高肠道内乳酸杆菌的水平,改善肠道屏障功能,从而减缓慢性肾病的进展。
AST-120这一非抗生素药物也显示出了显著的效果。AST-120通过减少肠道内的吲哚硫酸盐,改善肠道环境,并有助于减轻慢性肾病患者的症状。尽管这些药物的研究仍在进行中,但它们为慢性肾病的治疗提供了新的方向。
肾-肠轴的发现为慢性肾病的治疗提供了新的思路。通过调节肠道微生物群,改善肠道健康,我们可以有效减缓慢性肾病的进展。益生菌、益生元、后生元以及非抗生素药物的应用,正逐步成为慢性肾病治疗的重要组成部分。现有的临床证据仍不足以全面支持这些治疗手段的广泛应用,未来需要更多的大规模、长期的研究来验证其疗效和安全性。结合饮食干预和药物治疗的综合干预策略,或将成为慢性肾病治疗的未来方向。
主题测试文章,只做测试使用。发布者:,转转请注明出处:https://ly2s.net/article/xiongdaohang/11333.html


